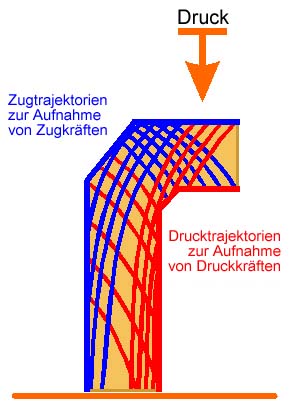
Trajektorielles Druck- und Zugspannungsverteilungprinzip, das z.B. im Röhrenknochen zur Wirkung kommt
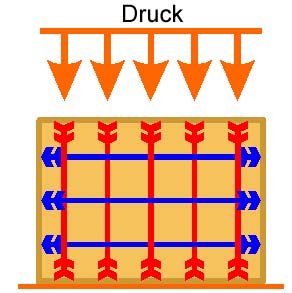
Trajektorielles Druck- und Zugspannungsverteilungsprinzip, das in platten Knochenstrukturen zur Wirkung kommt, dabei wirken Druckkräfte zentripedal
2 Knochen
2.1 Interzellularsubstanz.
2.2 Periost, Knochenhaut
2.3 Gefäß- und Nervenversorgung
2.4 Biologisches Verhalten
2.5 Leichtbauweise
2.6 Stoffwechsel und neuronale Beeinflussung durch intraossäre piezoelektrische Spannungen3 Knorpel
3.1 Knorpelaufbau
3.2 Hyaliner Knorpel4 Sehnen und Bänder
4.1 Struktureller Sehnenaufbau
4.2 Struktureller Bänderaufbau
4.3 Gelenkkapsel
4.4 Gelenkkapselaufbau
4.4.1 Membrana fibrosa
4.4.2 Gelenkinnenhaut
4.5 Gelenkband
4.6 Gelenkfläche
4.7 Gelenkhöhle5 Physiologisches Gelenk
5.1 Zusammenhalt
5.2 Führung und Hemmung der Gelenkbewegungen
5.3 Gefäß- und Nervenversorgung6 Bewegungshemmende und -fördernde Neuromechanismen
7 Biologische Gegebenheiten
7.1 Biologisch-physiologische Gegebenheiten
7.2 Biologisch-pathologische Gegebenheiten
7.2.1 Inaktivitätsfolgen
7.2.2 Altersveränderungen
7.2.3 Kapselläsionen
7.2.4 Bänderverletzungen
7.2.5 Knochenverletzungen
Hier sollen nicht die allgemein bekannten Erkenntnisse über Knochen, Knorpel und Gelenke dargestellt werden, sondern nur solche, die für die erweiterte Wirkungsweise manueller Arbeit an Gelenken im Sinne neural wirkender Reize von besonderem Interesse sind, initiiert doch eine entsprechende Dehnung nichtkontraktiler Strukturen in Gelenksbereichen in deren ganzem nervalen Innervationsbereich und in ihrem vaskulären Versorgungsgebiet reaktiv eine entsprechende Reizantwort, die Gelenksmobilisationen m. E. primär als Neurotherapie wirken lassen, wodurch sich deren über die mechanische Funktionsverbesserung hinausgehende positive Allgemeinwirkung erklärt.
Damit werden die Strukturen der knöchernen Gelenkspartner mit deren Gelenkkapsel, den Bändern und dem intraartikulären Gewebe bezeichnet. Ein Gelenk besteht aus einem knöchernen, einem knorpeligen und einem Band-Sehnen-Anteil.
[zurück zum Inhaltsverzeichnis]
Knochen weist Festigkeit gegen Zug,
Druck, Biegung und Torsion auf und hat die Fähigkeit, sich optimal
den an ihn gestellten Anforderungen anzupassen und ist zum Umbau
befähigt - Knochen lebt also.
Knochen besteht aus der zellhaltigen Hartsubstanz, aus dem Knochenmark
und einer bindegewebigen Hülle, dem Periost, das im Gegensatz zum
übrigen Knochengewebe eine reichere Gefäßversorgung
aufweist.
[zurück zum Inhaltsverzeichnis]
Zur Erreichung seiner Druckfestigkeit bilden die Osteoblasten, im synergistischen Antagonismus mit den Osteoklasten, in den interzellulären Substanzen der Knochen anorganisch kristalline Einlagerungen bei einem durchschnittlichen Kristalldurchmesser von 40 x 30 x 3 nm, die als Interzellularsubstanz parallel zu den dort formgebenden Kollagenfibrillen liegen und deren Oberfläche von einem Mantel gebundenen Wassers umgeben sind, wobei diese Bindegewebestruktur mit deren ca. einem Drittel bis der Hälfte des Gesamtgewichtsanteils der Knochensubstanz darin verfestigt ist. Diese Kristallstruktur baut sich auf aus ca. 85% ca. Kalziumphosphat, ca. 10% Kalziumcarbonat, ca. 1,5% Magnesiumphosphat, ca. 0,3% Kalziumfluorid, ca. 0,2 Kalziumchlorid und ca. 2% Alkalisalzen als Hydroxylapatit. Die organischen bindegewebigen Bestandteile des Knochens bestehen zu 95% aus Kollagenfasern, der Rest aus amorphen Interzellularsubstanzen, insbesondere neutrale und saure Mucosubstanzen neben den Osteozyten als den Knochenzellen und häufig auch Blutgefäßen.
[zurück zum Inhaltsverzeichnis]
Mit Ausnahme der
überknorpelten
Gelenkflächen sind die Knochen von Periost überzogen, das
sich in zwei funktionell ungleichwertige Schichten aufteilt, und zwar
in die hauptsächlich aus kollagenen Fasern bestehende derbe
äußere Schicht, das Stratum fibrosum, sowie in die zell- und
gefäßreiche innere Cambiumschicht. Das Stratum fibrosum ist
durch die Kollagenfaserbündel der Sharpey´schen Fasern, die
in die Substantia compacta eingewachsen sind, mit dieser verbunden. Um
im Bereich der Sehnen- und Bandansätze eine zu stark konzentrierte
Zugbeanspruchung des Knochens zu vermeiden, sind die kollagenen Fasern
der Sehnen nur zum Teil direkt in die Knochensubstanz eingewachsen, zum
anderen Teil sind sie breit im Stratum fibrosum inserierend, um dadurch
die über sie am Knochen angelenkten Zugkräfte auf eine
möglichst große Fläche zu verteilen.
Die für den Knochenstoffwechsel wichtige Cambiumschicht
enthält zahlreiche kleine Gefäße und Kapillaren zur
Versorgung der Volkmann´schen und Havers´schen
Gefäße zur Ernährung der Knochensubstanz. Aus der
Cambiumschicht entstehen während der knöchernen Entwicklung
die Osteoblasten, welche für das Wachstum des Knochens in seiner
Stärke verantwortlich sind. Nach Beendigung des Wachstums bleibt
diese Osteoblastenbildung aus, wodurch sich die Produktion von
Knochensubstanz einstellt, außer wenn nach einer Fraktur die
Regenerationsphase einsetzt, wodurch aus der Cambiumschicht erneut
Osteoblasten entstehen und die Knochenfragmente zunächst in einen
zell- und faserreichen Kallus eingeschlossen werden, in dem sich
bereits nach wenigen Tagen Knochengewebe bildet. Durch diese Bildung
von neuer Knochensubstanz kommt es zu einer äußerst stabilen
Überbrückung des Frakturspaltes durch Geflechtknochen, der
sich später zu Lamellenknochen umbaut.
[zurück zum Inhaltsverzeichnis]
Die Knochensubstanz wird über
die
Blut- und Lymphgefäße sowie durch die Nerven des Periosts
versorgt. Größere Gefäße, Vasa nutricia, dringen
durch gleichnamige Foramina in die Markhöhle vor und versorgen das
Knochenmark.
Wie bei der Versorgung der Knochensubstanz verhält es sich mit den
Gefäßen, welche den Epiphysenbereich der Röhrenknochen
zur Ernährung der Spongiosa und des Marks versorgen.
Nervenfasern sind im Periost und in den Kanälchensystemen der
Knochensubstanz nachgewiesen. Ihre besondere Bedeutung liegt in der
sensiblen Innervation des Periosts. Verletzungen des Periosts sind
äußerst schmerzhaft.
[zurück zum Inhaltsverzeichnis]
Im Gegensatz zum Knorpelgewebe ist
die
Knochensubstanz gut vaskularisiert, die Durchblutung, und damit der
Stoffwechsel, ist dazu vergleichsweise hoch.
Auch wenn das Knochengewebe als widerstandsfähige Hartsubstanz
erscheint, erfolgt auch beim Erwachsenen, unter Aufrechterhaltung der
äußeren Form des Knochens, ein ständiger innerer
Gewebsumbau in einzelnen Haver´schen Lamellensystemen. Auch zeigt
der Knochen, ebenso wie die Muskulatur, eine Anpassung an sich
verändernde mechanische Belastungen - funktionelle Anpassung. So
führt eine vermehrte systemgerechte, über die Gelenkenden
wirkende Belastung z. B. bei Röhrenknochen zu einer Verdickung der
Compacta und der Spongiosa als Form einer Aktivitätshypertrophie.
Umgekehrt schwindet Knochenmaterial bei allgemeinen Bewegungs- und
Belastungsinaktivitäten in Art einer knöchernen
Inaktivitätsatrophie, die im Röntgenbild durch eine zarte
Spongiosazeichnung zu erkennen ist. Die Knochenatrophie ist auch eine
der typischen Altersveränderungen beim Menschen, die eine
erhöhte Frakturgefährdung zur Folge hat.
[zurück zum Inhaltsverzeichnis]
Eine der bemerkenswertesten
Eigenheiten
des menschlichen Skeletts ist seine Erschaffung in der ihm eigenen
Leichtbauweise, die, wie bei allen auf dem Land lebenden Wirbeltieren,
hohen mechanischen Beanspruchungen genügend
Stabilitätssicherheit entgegenzusetzen vermag, dessen Vorteil im
Sinne des biologischen Ökonomieprinzips und in der Einsparung von
Stoffwechselenergie liegt, denn eine reduzierte Knochenmasse hat
geringeren Eigenbedarf für ihre Ernährung und einen ebenso
geringeren Bewegungs- und Haltekraftaufwand, wodurch der gesamte
Energieaufwand für dessen Funktion sich reduziert.
Die Leichtbaukonstruktion ist beim Landsäugetier und beim
Menschen, wie in technischen Systemen auch, auf zwei Arten erreicht
worden: Durch Verwendung von Baumaterial mit hochwertigen mechanischen
Eigenschaften - so findet sich beim Menschen fast ausschließlich
der Lamellenknochen, der eine höhere Druck-, Zug- und
Biegespannungsfestigkeit besitzt als der Geflechtknochen - und durch
die trajektorielle Bauweise mit der Anordnung des Stützmaterials
entgegen den größten Druck- und Zugspannungen (als
Trajektorien werden in der Technik jene Linien bezeichnet, die an den
Stellen eines belasteten Körpers die Richtungen des
größten Drucks oder des größten Zuges angeben -
ein solches trajektorielles Bauprinzip besteht nach bisherigen
Erkenntnissen und Untersuchungen in der gesamten Spongiosastruktur des
menschlichen Skeletts). Die Spongiosabälkchen sind beim
menschlichen Skelett dermaßen angeordnet, dass sie dem Verlauf
der größten Druck- oder Zugspannungen entsprechend axial auf
Druck oder Zug beansprucht werden können.
|
|
|
|
Trajektorielles Druck- und Zugspannungsverteilungprinzip, das z.B. im Röhrenknochen zur Wirkung kommt |
Trajektorielles Druck- und Zugspannungsverteilungsprinzip, das in platten Knochenstrukturen zur Wirkung kommt, dabei wirken Druckkräfte zentripedal |
[zurück zum Inhaltsverzeichnis]
Dieser Effekt findet sicherlich zu wenig Beachtung, ist aber nach meinem dafürhalten wohl einer der wichtigsten überhaupt in der Stoffwechsel- und Reizleitungsmechanik, die in Knochenstrukturen und den von diesen ausgehenden Reizen zur Wirkung kommen. Zug- und Druckspannungen der Knochenstrukturen lösen piezoelektrische Reaktionen aus die immer dann entstehen, wenn kristalline Strukturen unter Druck- oder Zugbelastungen kommen (dieser elektrophysikalische Effekt wird z. B. genutzt in Schallplattentonabnehmern älterer Bauart, den sogenannten "Kristallsystemen“, oder bei den bekannten batterielosen Piezozündern für die Gasentzündung an Herden und in Heizungsanlagen). Durch diese Reizkomponente werden möglicherweise reflektorische muskuläre An- bzw. Verspannungen über Nozizeptive Somatomotorische Blockierungseffekte ausgelöst, die dann reaktiv im Knochen auftretenden Biegespannungen entgegenwirken. Andererseits beeinflussen sie wohl auch die Osteoblasten- und Osteoklastenaktivitäten. Das elektrische Spannungsgefälle, das zwischen der Kristallspitze und dem Kristallinneren der kristallinen Knochenstrukturen besteht, vermag einen elektrischen Strom in der Größenordnung von ~ 1 Femtoampère (= ~ 10-15 Ampère) unter der reizleitungserregten Spannung von ca. 70 mV auszulösen, wobei durch diesen Strom unter Druckspannung stehende Kristalle als Kathode, unter Zugspannung stehende als Anode wirken. So gelangen Kalziumionen zum negativen Pol und können dabei von den Osteoblasten in die Knochenmatrix eingebaut werden. Dadurch verschieben sich diese Kalziumionen zur Seite des Druckspannungsbereichs, so dass das Knochengewebe auf jener Seite sich verstärkt. Dieser Vorgang findet überall dort statt, wo der Knochen höheren Druckbeanspruchungen ausgesetzt ist bzw. bei Belastungen Druckspannungsspitzen entstehen wie z. B. im Bereich unphysiologisch a-achsengerecht belasteten Gelenken oder bei Knorpeldefekten, wo Druckeinwirkungen nicht mehr gleichmäßig auf die Umgebung verteilt und übertragen werden.
[zurück zum Inhaltsverzeichnis]
Knorpel besteht aus organischem Material. Eine besondere Eigenschaft des Knorpels ist seine Druckelastizität, was bedeutet, dass Knorpel bis zu einem gewissen Grade komprimierbar, aber auch dehnbar, ist. Beim Nachlassen der Druck- und Zugkräfte gewinnt Knorpel seine Ausgangsform wieder. In Gelenken begünstigt der Knorpel das Gleiten der Skeletteile gegeneinander.
[zurück zum Inhaltsverzeichnis]
Die Chondrozyten und Chondroblasten
als
Knorpelzellen enthalten in ihrem Zytoplasma, dem Hyaloplasma,
Fetttröpfchen, Mukoproteïd, Granula und reichlich Glykogen.
Knorpelzellen und -hülle werden zusammen als Knorpelkugel bzw.
Chondrom bezeichnet. Die Organellen sind mit Enzymsystemen
ausgestattet, die besonders für den anaeroben Abbau des Glykogens
sowie den Auf- und Abbau der
Polysacharide, Chondroitinschwefelsäure und Hyaluronsäure
zuständig sind, aus denen der Knorpel neben kollagener Substanz,
wasserlöslichen Aminosäuren und Mineralien besteht.
Einzeln oder gruppiert sind die Chondrozyten und Chondroblasten in eine
kollagene Fasergrundsubstanz eingewickelt, die mit einer
hyaluronsäurereichen Kittsubstanz "verbacken“ ist.
In den knochennahen intensiver vaskularisierten und dadurch
sauerstoffreichen Knorpelanteilen ist die Anwesenheit von
Atmungsfermenten, den Zytochromen, für den aeroben Stoffwechsel
verantwortlich. Während im Knorpel Energieträger und
Aufbaustoffe für dessen Kernsubstanz in diesen
gefäßversorgten Abschnitten aus der Blutbahn bezogen werden,
werden sie in den nicht vaskularisierten Knorpelregionen durch
Diffusion und Osmose aus dem Umgebungsgewebe, insbesondere aus der
Synovia, beschafft. Die Tätigkeit der Chondrozyten wird endokrin
beeinflusst, z. B. gesteigert durch Thyroxin, Testosteron und gehemmt
durch Cortison und Östradiol.
Der Wassergehalt des Knorpels nimmt im Alter ab, womit ein Nachlassen
der Druckelastizität verbunden ist. Gleichzeitig kann es zu einer
Verminderung der Knorpelgrundsubstanz kommen, so dass eine sog.
"Asbestfaserung“ auftritt. Ferner kann es zu einer Zystenbildung im
Knorpel und zu Verkalkungen kommen.
Die physikalische Eigenschaft des Chondroms ist vergleichbar mit einem
wassergefüllten prallelastischen Kissens, das auf Druck nach jeder
Seite einen Druckausgleich ermöglicht (dies ist auch ein
Teilanwendungsprinzip des Therapie-Kissens nach Horn®), wobei die
Faserelemente auf Zug beansprucht werden und das dichte Faserwerk von
Wicklungen der einzelnen Knorpelkugeln sowie der verschiedenen
Knochenkugeln miteinander dem Knorpelgewebe seine ganz hervorragende
Druckfestigkeit verleihen können - die Anordnung der
Kollagenfasern im einzelnen ist den jeweiligen funktionellen
Ansprüchen angepasst (im Sinne von Trajektorien). So verlaufen
beispielsweise im Gelenkknorpel die Kollagenfasern bogenförmig von
der Knorpel-Knochengrenze zur freien Oberfläche, wo sie sich
tangential orientieren. Im Rippenknorpel, der vor allem auf Biegung
beansprucht wird, verlaufen die Kollagenfasern S-förmig durch die
Interzellularsubstanz. Unter den Oberflächen münden sie in
Tangentialfaserschichten ein. Die eigentliche Druckschicht im Knorpel
ist die Außenzone, dort gehen die Kollagenfasern in das
Perichondrium, eine Faserschicht, über.
[zurück zum Inhaltsverzeichnis]
Beim Cartilago hyalina, dem
eigentlichen
Gelenkknorpel und die Knochenwachtumsgrundstruktur im Embryonal- und
Wachstumsstadium für die meisten Skelettknochen, finden sich in
den oberflächlich gelegenen Keimschichten der Gelenkknorpel die
Knorpelkugeln dicht beieinanderliegend sowie untereinander mit
Kollagenfasern verbunden, wobei in der tieferen Knorpelschicht die
Knorpelkugeln im Verhältnis dichter gepackt sind als in den
oberflächigen, die zur Gelenkhöhle hin durch das
Perichondrium abgegrenzt sind. Beim Perichondrium handelt es sich um
das umgebende Gewebe hyaliner Knorpel in Form einer Knorpelhaut, das an
der Knorpeloberfläche sehr zellreich (Stratum cellulare), weiter
außen mehr faserreich (Stratum fibrosum) ist. Vom Perichondrium
her bildet sich Knorpelsubstanz neu, es ist gefäß- und
nervenreich.
Das Vorkommen hyaliner Knorpel ist in den Luftwegen (als Knorpelspangen
in der Trachea und Knorpelstückchen in den Bronchien),
Nasenknorpel, knorpeliger Anteil der Rippen und, wie bereits
erwähnt, beim Knochenwachstum und an Gelenken als Gelenkknorpel.
[zurück zum Inhaltsverzeichnis]
Sehnen und Bänder, Knorpel, Knochen und Denti bestehen aus Stützgewebe und sind in erster Linie geordnet geformtes und formendes Bindegewebe. Sie zeichnen sich durch Interzellularsubstanzen größerer Festigkeit aus, dadurch haben Stützgewebe eine Eigenform, können Weichgeweben einen Halt geben und Schutzfunktionen ausüben.
[zurück zum Inhaltsverzeichnis]
In Sehnen verlaufen die
Kollagenfasern
parallel, in großen Sehnen häufig in leichten Spiralen. In
ungedehntem Zustand sind die Kollagenfaserbündel leicht gewellt.
Zwischen den Kollagenfasern als Sehnenfasern liegen in Reihenstellung
hintereinander angeordnet Fibrozyten, die Sehnenzellen. Diese Zellen
haben langgestreckte Kerne und wenig Cytoplasma. Sie passen sich in
ihrer Form der Umgebung dadurch an, dass ihr schmal ausgezogenes
Cytoplasma "flügelartig“ den Sehnenfasern anliegt
("Flügelzellen“).
Sehnen werden von lockerem Bindegewebe umhüllt, dem Peritendineum
externum, das in das Innere der Sehne eindringt (Peritendineum
internum) und kleinere primäre Bündel und größere
sekundäre Bündel
zusammenfasst. Mit dem lockeren Bindegewebe dringen Nerven und
Blutgefäße in die Sehne ein.
Sehnen haben eine gute Regenerationsfähigkeit. In Bändern,
Faszien und Aponeurosen verlaufen die Kollagenfaserbündel nach
einem festgelegten Muster, das der Zugbeanspruchung angepasst ist. In
der Sklera beträgt der Winkel zwischen den einzelnen
Faserbündeln nahezu 90 Grad.
[zurück zum Inhaltsverzeichnis]
Das elastische Band besteht aus Bündeln dicker, parallel angeordneter elastischer Fasern. Jedes Bündel umfasst geringe Mengen lockeren Bindegewebes mit abgeplatteten Fibrozyten. Die elastischen Fasern rufen in frischem Gewebe eine gelbe Farbe hervor. Beim Menschen kommen geschlossene elastische Bündel in den Ligg. flava der Wirbelsäule und im Lig. suspensorium penis vor.
[zurück zum Inhaltsverzeichnis]
Die Capsula articularis schließt das Gelenk allseitig ein und kann als schlauchförmige Fortsetzung des Periosts angesehen werden.
[zurück zum Inhaltsverzeichnis]
An ihrer Außenseite weist die Gelenkkapsel fibröses Gewebe auf mit eingelagertem vaskularisiertem Bindegewebe. So besteht die Gelenkkapsel, wie das Periost auch, aus zwei Faserschichten, und zwar aus der
[zurück zum Inhaltsverzeichnis]
- bei den einzelnen Gelenken unterschiedlich stark ausgebildet mit deren kräftigen Bündel- oder Zugstrukturen aus kollagenen Fasern, an denen auch einstrahlende Sehneninsertionen beteiligt sein können, die Ligg. articularia - und der
[zurück zum Inhaltsverzeichnis]
- Membrana synovialis -, bestehend aus lockerem Bindegewebe mit variablem Gehalt an Fettzellen, an deren innerer Oberfläche die sonst verzweigten Fibrozyten flächenhaft ausgebreitet sind - sie bieten somit histologisch das Bild eines einschichtigen, zuweilen auch mehrschichtigen Epithels. Die Membrana synovialis bildet gefäßreiche Falten sowie fettzellenhaltige vaskularisierte Zotten und enthält außerdem zahlreiche Nervenfasern und Rezeptoren. Die Zotten und Falten neigen zur Verkalkung, beim Abreißen dieser kalzifizierten Gebilde infolge einer forcierten Gelenkbewegung werden sie dann als freie Gelenkkörper eingeklemmt, wodurch es zu einer äußerst schmerzhaften Sperre des Gelenks kommt.
[zurück zum Inhaltsverzeichnis]
Das Lig. articulare ist ein
wichtiges
Element des Gelenks und weist, wie die Sehnen auch, eine straffe
Struktur aus weitgehend parallel orientierten kollagenen Fasern auf.
Meist sind die Ligg. articularia in die Membrana fibrosa der
Gelenkkapsel eingeflochten als Verstärkungsbänder,
können aber auch autonom die artikulierenden Knochen miteinander
verbinden.
Die Aufgaben der Gelenkbänder sind erstens das Sichern der
Führung der Gelenke in deren physiologischen Bewegungsbahnen und
zweitens begrenzen sie die Gelenkexkursionen zur Verhinderung
unphysiologischer Bewegungsausschläge.
[zurück zum Inhaltsverzeichnis]
Die Facies articularis ist je nach
Gelenk
unterschiedlich geformt. Die Gelenkflächen besitzen einen
Knorpelüberzug, wobei knorpelig präformierter Knochen an
diesen als Rest des embryonalen Knorpels aus hyalinem Knorpel besteht.
Sind Deckknochen gelenkig miteinander verbunden wie im Kiefergelenk,
besteht der Gelenksknochenüberzug aus Faserknorpel. Dem
Gelenkknorpel fehlt faseriges Perichondrium, wodurch seine
Oberfläche eine glatte Struktur aufweist, wobei stark
druckbelastete Gelenkflächen einen besonders dicken Knorpelbelag
haben wie z. B. am Kniegelenk mit einer Stärke von bis zu 5 mm.
Bei inkongruenten Gelenkflächen spielt die Verformbarkeit des
Knorpels eine wichtige Rolle, da die Kontaktflächen der
Gelenkenden mit steigendem Druck ständig größer werden
und die Druckverteilung sich bei elastischem Gelenkknorpel entsprechend
verbessert.
Die Primärbeanspruchung des Gelenkknorpels auf Druck- sowie
Scherkräfte kommt auch in seinem histologischen Aufbau zum
Ausdruck, denn die kollagenen Fibrillen steigen von der
Knorpel-Knochen-Grenze etwa rechtwinkelig zur Knorpeloberfläche
auf und enden gebogen in dessen oberflächiger Tangentialschicht.
[zurück zum Inhaltsverzeichnis]
Die Cavum articulare ist im eigentlichen Sinn keine Höhle, sondern ein kapsulärer Spalt, der lediglich eine geringe Menge Gelenkschmiere, Synovia, enthält, die, wie auch das Schmiermittel in technischen Gelenken, als Gleitmittel fungiert und eine gewisse Ernährung des gefäßlosen Gelenkknorpels ermöglicht. An der Bildung dieser schleimartigen mucopolysacharidhaltigen Flüssigkeit sind die Fibrozyten der Synovialis beteiligt.
[zurück zum Inhaltsverzeichnis]
Diese Bezeichnung meint das Gelenk als anatomische Funktionseinheit mit den dazugehörigen Weichteilen, der vaskulären Versorgung und der entsprechenden Innervation.
[zurück zum Inhaltsverzeichnis]
Für den Kontaktschluss der Gelenkflächen sind äußere Kräfte verantwortlich, hier an erster Stelle Zugkräfte der über das betreffende Gelenk hinwegziehenden Bänder, Sehnen und Muskeln, an den unteren Extremitäten zusätzlich das Körpergewicht - neben den inneren Adhäsions- und Vakuumkräften im Gelenk, die dieses sich regelrecht "zusammengesaugt“ sein lassen.
[zurück zum Inhaltsverzeichnis]
Eine gebahnte Bewegungsführung
und
Bewegungshemmung in bestimmten Extremstellungen ist für die
Funktionstüchtigkeit der Gelenke unerlässlich, ein
Schlottergelenk ist funktionell wertlos.
Die regelrechte Gelenkbewegungsführung und -hemmung nach lateral
zum Bewegungsradius und in den endgradigen Stellungen erfolgt durch den
jeweiligen Bandapparat - ligamentäre Komponente - und die das
Gelenk beeinflussende Muskulatur - muskuläre Komponente - in
unterschiedlichem Maße, bei einigen Gelenken noch zusätzlich
durch die Knochen mit ihren Gelenkflächen - ossäre oder
knöcherne Komponente -, wobei die zuletzt genannte
Gelenkführungsart jenen Gelenken mit besonders dafür
geformten Gelenkflächen gegeben ist wie z. B. dem Hüft- und
oberen Sprunggelenk, etwas auch dem Iliosakralgelenke. Eine
knöcherne Bewegungshemmung kommt ansonsten nicht vor, allenfalls
z. B. bei gewaltsamer Überstreckung im Ellenbogengelenk.
Die Bänderführung hat große Bedeutung bei Gelenken mit
stark inkongruenten Gelenkflächen wie z. B. dem Kniegelenk,
Gelenke mit planen Gelenkflächen wie den Hand- und
Fußwurzelgelenken, solchen mit semiplanen Gelenkflächen wie
dem Iliosakralgelenke, dem Rad- bzw. Zapfengelenk und bei
Scharniergelenken. An die Stelle der bei diesen Gelenken fehlenden
Knochenführung tritt die führende Funktion des betreffenden
Bandapparates mit seiner ligamentären
Bewegungsführungsaufgabe, Gelenkbewegungen nur in bestimmten
Richtungen zu ermöglichen. Eine Bänderhemmung ist funktionell
sehr wichtig. In vielen Gelenken, wie beispielsweise den Hüft-,
Knie- und Ellenbogengelenken sowie den Finger- und Zehengelenken, wird
deren Extension ausschließlich durch die ligamentäre
Haltefunktion gehemmt. Die Muskelführung ist bei jenen Gelenken
erforderlich, deren ausgeprägte Bewegungen weder ossär noch
ligamentär gesichert ist wie am Schultergelenk. Die Muskeln haben
dabei die Funktion von sich "verstellenden“ Bändern bei deren
muskulärer Bewegungsführung.
Eine Muskelhemmung liegt dann vor, wenn bei bestimmten
Gelenksendstellungen die Dehnbarkeit eines darüberziehenden und
dieses Gelenk beeinflussenden mehrgelenkigen Muskels oder einer
Muskelgruppe erschöpft ist. Solch eine Weichteil- oder
Massenhemmung tritt z. B. bei extremer Beugung im Ellenbogen- oder
Kniegelenk in Funktion.
[zurück zum Inhaltsverzeichnis]
Die arterielle Gelenkversorgung wird meist durch einen Gefäßring um die Gelenkkörper gebildet, dessen Äste auch die Epiphysen und die Gelenkkapsel erreichen, wobei die Synovialmembran besonders reich kapillarisiert ist.
[zurück zum Inhaltsverzeichnis]
Im Stratum fibrosum der Kapsel und
im
Umgebungsgewebe finden sich zahlreiche afferente Nervenfasern für
die Tiefensensibilität, besonders zur Schmerzrezeption. Die
Gelenkkapsel ist mit einem fein verzweigten Netz von sensiblen
marklosen und markhaltigen Nervenfasern durchsetzt, die in der Lage
sind, chemische, mechanische, thermische, osmotische und onkotische
Reize zu registrieren. Die Nervenfasern finden sich sowohl im Stratum
fibrosum als auch im Stratum synoviale. Die Faserführung erfolgt
entlang der Gefäße, teilweise zu den Muskeln, teilweise zu
den Gelenken. Auf ihrer Endstrecke teilen sie sich auf und ziehen zu
den bindegewebigen Zellen der Synovialmembran und zu den Kapillaren. In
den Gelenkkapseln und in den Bändern finden sich die sogenannten
Ruffini-Endorgane, den Muskelspindeln ähnlich, zur Registrierung
von Gelenkbewegungen über verschiedene Winkelbereiche und genauen
Meldung von Gelenkstellungen an das Zentralnervensystem, wodurch diesem
ein exaktes Bild der Gelenkstellungen übermittelt wird. Dabei
fällt den Propriozeptoren der Gelenkkapsel und der Ligamente die
selbe Funktion zu wie im Bereiche der Muskeln, wo deren Afferenzen
über Zwischenneuronen zu den Motoneuronen im Vorderhorn der
Agisten, Synergisten und Antagonisten sowie zu den Integrationszentren
geleitet werden, wodurch es zur Anpassung von Anspannungen der dazu
antagonistischen Muskeln als der Situation adäquaten
kapsulären Beanspruchungen der Gelenke und Knochen kommt. Durch
diese Sensomotorik wird der geordneter Bewegungsablauf in den
Gelenksbereichen ermöglicht wie auch durch das selbe System mit
seinen Rezeptoren in den Knochen die tonische Anpassung der Muskulatur
mit ihrer Zuggurtenfunktion möglich ist.
Bei der Betrachtung der Nozizeptoren und deren Bedeutung muss hier auf
die ausgedehnten und ausführlichen Arbeiten von BRÜGGER,
Zürich, verwiesen werden zu dem Globalthema Nozizeptiver
Somatomotorischer Blockierungseffekt - NSB. Dr. med. ALOIS
BRÜGGER, Neurologe, hat hier echte Grundlagenforschung betrieben,
ohne deren Kenntnis der in der Physiotherapie tätige Therapeut m.
E. keine sinnvolle Therapie auszuführen in der Lage ist (auch wenn
die praktische Anwendung der von BRÜGGER erarbeiteten
Therapieansätze und ergonomischen Empfehlungen nicht nur mir in
einigen Punkten so weit zu gehen scheinen, dass zum Nutzen einiger
Komponenten andere Schaden leiden können). Die im folgenden
gemachten Ausführungen stützen sich neben eigenen
Erkenntnissen ansonsten ausnahmslos auf Arbeiten und Ausarbeitungen
BRÜGGERs, auf dessen Fachbuch "Die Erkrankungen des
Bewegungsapparates und seines Nervensystems", G. Fischer-Verlag
Stuttgart-New York, an dieser Stelle als Standardwerk
neurologisch-neurophysiologischer Literatur verwiesen sei.
Aktivitäten der Nozizeptoren hemmen die Aktivitäten der
Motoneurone, bei vorliegen starken Zerrungen am Gelenkkapsel- und
-bandapparat kann es zu einer reaktiven vorübergehenden mehr oder
weniger ausgeprägten "funktionellen“ Lähmung kommen, die
beispielsweise im Schulter-Armbereich als Chassaignac-Syndrom bekannt
ist. In anderen Fällen ruft die Nozizeptorenaktivität
umgekehrt eine hochschmerzhafte Hypertonie der Muskulatur hervor, wie
dies bei Überlastungsfolgen und akut infektiösen, stark
schmerzhaften Bursitiden auftreten kann und der diese begleitende
muskuläre Hartspann dabei schmerzhafter als die Bursitis selbst
sein kann durch nozizeptorengeförderte Aktivitäten peripherer
motorischer Neurone. In diesen Fällen werden gleichzeitig die
antagonistischen Muskeln mit entgegengesetzt zur
symptomverstärkenden Bewegung wirkendem Funktionssinn
beeinflusst.
Von den Gelenkkapseln können stärkste hemmende Impulse auf
die Muskulatur ausgelöst werden, wie z. B. Gelenkkapseln
frühzeitig und intensiv Nozizeptorenaktivitäten auslösen
können als schmerzhaft zu verspürende Aktion - ein
Gelenkreizzustand ist Ausdruck eines nozizeptiv irritierten
Gelenkkapselapparates -, was jedoch über die Gelenkreizursache
nichts aussagt, da diese in einen solchen Reizzustand bei den meisten
Fehl- oder Überbeanspruchungen verfallen können,
auslösbar durch alle pathologischen Prozesse, welche das
Gelenksgewebe zu schädigen vermögen, wie z. B.
Entzündungen oder Verletzungen.
Reizzustände eines Gelenkes induzieren beispielsweise u. U. eine
reflektorische Verspannung der Muskeln, welche dieses bewegen und
führen. Wird hier in einem solchen Fall z. B. massiert,
können sich die Schmerzen verstärken. Im Gegensatz dazu
wirken antiphlogistische Maßnahmen (Kryotherapie als langzeitige
Kälteeinwirkung bis zu 20 Minuten, kurze "getupfte“
Hitzeanwendung, Elektrotherapie bzw. Iontophorese mit Antiphlogistika
etc.) im Bereich des betreffenden Gelenkes, das Ursache der
ausgelösten Nozizeptorenaktivität ist, beschwerdelindernd.
Pathophysiologischen gegenregulatorischen Mechanismen des Körpers
liegt das Ziel der Schonung des Reizherdes zugrunde. Die
Entlastungshaltung als Schonhaltung für das betreffende Gelenk
reduziert den mechanischen Faktor für die Auslösung bzw.
Intensivierung der arthrogenen Schmerzimpulse. Nozizeptive Reize hemmen
daher jene Muskeln, die den Reizherd verstärken. Gleichzeitig
damit werden aber auch jene Muskeln erfasst, deren Kontraktion der
Schonung dienen - der Gelenkschonung dienende Muskeln werden
reflektorisch in einen hypertonen bis kontrakten Zustand versetzt,
wobei Fibrillationen auftreten können und Muskelanteile in
Veränderungen, z. B. in Form von Myogelosen, übergehen
können. Die betroffenen Gelenkkapseln neigen zur Schrumpfung in
den eingenommenen Schonhaltungen. Die Folge ist einer sekundäre
Gelenksteife in Schonhaltung, die teils kapsulär, teils
muskulär bedingt ist. Ein Beispiel für eine solche
Neuromechanik stellt die Gruppe des M. iliopsoas dar, welche bei einer
Coxarthrose durch eine erhöhte Dauerkontraktion von anterior das
Hüftgelenk ruhigstellt (daher kommt auch der bei
Hüftgelenksarthrosen typische Leistenschmerz im Bereich der Lacuna
musculorum). Da, wie bereits erläutert, ein zu hoher Reflextonus
der Muskulatur zu weiteren sekundären Komplikationen führen
kann wie z. B. zu Myogelosen oder mikrotraumatischen Folgen
tendoperiostaler Belastung, können dadurch neue
pathofunktionsinduzierende Nozizeptorenaktivitäten ausgelöst
werden, die ihrerseits das Krankheitsbild im sinne eines Circulus
vitiosus unterhalten. Sind diese als solche erkannt worden, so
müssen sie direkt, nicht ihre Begleitsymptome, ausgeschaltet
werden, damit der nozizeptive somatomotorische Reflextonus herabgesetzt
werden kann.
Sehnen und Sehnen-Periostinsertionszonen sind mechanischen
Überbeanspruchungen mit den Folgen von Tendopathien bzw.
Tendoperiostosen exponiert ausgesetzt, in deren Zusammenhang es zu
Insertionsläsionen mit kleinen subperiostalen Blutungen und
reaktiven Infiltrationen des Periostes kommen kann, wie auch
Druckbelastungen, entzündliche Veränderungen und traumatische
Verletzungen Nozizeptorenaktivitäten auslösen mit
entsprechenden Sehnenreizzuständen. Deshalb setzen Reize an den
Sehnenspindeln die Aktivität an jenen Muskeln herab, welche die
betreffenden Sehnen zur Kraftübertragung nutzen.
Der Gleitapparat des arthromuskulären Komplexes kann ebenso ein
Pathoreflexauslöser sein z. B. durch mechanische Scheuerprozesse
und entzündliche Erkrankungen, welche Nozizeptorenaktivitäten
bedingen.
Nozizeptorenaktivitäten schmerzhafter Sehnen nehmen zu, wenn sich
deren zugehöriger Muskel kontrahiert, wodurch dieser, wie wir es
bereits betrachtet haben, reflektorisch hypoton und adynam wird =
reaktive Hypotonie des den Reizzustand verstärkenden Muskels -
hyperton werden jene Muskeln, die der Schonung des Reizherdes dienen.
Natürlich können auch Muskeln Nozizeptorenaktivitäten
induzieren in Folge beispielsweise von Muskelverletzungen, lokalen
mechanischen Druckeinwirkungen, intramuskulären entzündlichen
Prozessen, ischämischen und hypoxämischen Zuständen. Es
steht jedoch die akut pathogenetische Bedeutung der Muskulatur hinter
jener der Gelenke und Sehnen. Dafür spielt aber der Muskel als
Erfolgsorgan des NSB eine zentrale Rolle, wodurch es zu erheblichen
muskelinduzierten Systemstörungen kommen kann, wie dies die
neueren Arbeiten zur Problematik der Fibromyalgie zeigen, die
allerdings auf Grund von unterschiedlichen fachspezifischen
Betrachtungsweisen, mit denen an diese Problematik herangegangen wird,
derzeit noch nicht interdisziplinär spezifiziert scheint.
Auch Knochen können Nozizeptorenaktivitäten auslösen in
der Folge von deren Entzündung, aber auch durch mechanische
Überbeanspruchungen wie erhöhte Zug- und, mehr noch,
Biegespannungen als Belastungsspannungsspitzen.
[zurück zum Inhaltsverzeichnis]
Die biologischen Grundmuster der Gelenke sind genetisch festgelegt, doch sind sie einzelgelenkspezifisch durch die jeweilige Gelenksfunktion darauf abgestimmt modifiziert. Durch Training kann der Bewegungsumfang im Gelenk gesteigert werden und die überknorpelten Berührungsflächen breiten sich dadurch entsprechend aus. Gleichzeitig vergrößern sich belastungsrelevant Gelenkkapselabschnitte, Bewegung hemmende Bänder verlängern sich.
[zurück zum Inhaltsverzeichnis]
Die länger andauernde Ruhigstellung eines Gelenkes führt an dessen kollagenen Strukturen zu einer mehr oder minder ausgeprägten Kontraktur der Kapsel und des Bandapparates. Sofern größere Reservefalten an der jeweiligen Gelenkkapsel vorhanden sind, "verklebt“ deren Synovialmembran. Die sich aneinanderlegenden Kapselfaltenoberflächen bestehen aus Fibrozyten, die dabei, aus ihrem Epithel-artigen Verband gelöst, unter Neubildung kollagener Fibrillen eine Verklebung bis zu einer Verschmelzung deren synovialer Oberfläche verursachen und dadurch die physiologische Bewegungen mehr oder weniger einschränken.
[zurück zum Inhaltsverzeichnis]
In Folge mangelnder Bewegung und unphysiologischer Belastung schränkt sich der Gelenksbewegungsumfang mit zunehmenden Lebensjahren mehr und mehr ein. Regressive Veränderungen des gefäßfreien Gelenkknorpels führen zu dessen Abflachung und zur Asbestdegeneration. Zunehmend kommt es an den Randpartien des Gelenkknorpels zuweilen zu Knorpelproliferationen, die kalzifizieren können und später ossifiziert dem Knochengewebe ähnlich werden. Diese Veränderungen können bei ständiger Überbelastung oder Fehlbelastung der Gelenke selbst in jüngeren Lebensjahren auftreten (als klinischer Hinweis mag anzusehen sein, dass unter den Erkrankungen und Verletzungen des Bewegungsapparates Gelenkschäden relativ häufig sind in Folge von Unfall- und Sportverletzungen, rheumatischen und degenerativen Prozessen).
[zurück zum Inhaltsverzeichnis]
Bei der Verstauchung und Zerrung, also der Distorsion oder bei der Prellung (Kontusion) im Gelenkbereich ist die Gelenkkapsel besonders betroffen. Sie reagiert, je nach Stärke der Gewalteinwirkung, mit Schwellung oder vermehrter Flüssigkeitsabsonderung in die Gelenkhöhle als Gelenkserguss, aber auch, falls Kapselgefäße zerreißen, mit Blutaustritt in die Gelenkhöhle in Hämatomform. Entsprechend schmerzender Nervenreiz und Mehrdurchblutung sind die Folge, so dass sich hierbei mehr oder weniger alle Komponenten einer abakteriellen Entzündungsreaktion einstellen, welche sich ja bekanntlich durch die Komponenten Kalor, Dolor, Rubor und Tumor auszeichnet.
[zurück zum Inhaltsverzeichnis]
Bei oben genannten Traumen sind häufig auch die Gelenkbänder beteiligt, da sie bei den meisten Gelenken in die Kapselstruktur eingewachsen sind. Eine Bänderläsion ist vor allem dann wahrscheinlich, wenn äußere Kräfte eine durch Bänder gehemmte Gelenkbewegung unphysiologisch forcierten, wie z. B. bei einer unphysiologischen Hyperextension im Ellenbogen- oder Kniegelenk. Dabei gibt es verschiedene Verletzungsgrade von der einfachen Bänderzerrung bis zum kompletten Bänderriss.
[zurück zum Inhaltsverzeichnis]
Wegen der ausgeprägten
Zugfestigkeit
kollagener Fasern bleibt bei einer traumatisierenden
unkontrolliert-überdimensionierten Gelenksbewegung die
Kontinuität kräftiger Bänder meist erhalten, so dass es
statt einer Bänderläsion oder -ruptur zu einem Abriss des
Knochenabschnittes kommt, in den das Band inseriert wie beispielsweise
bei einer Abrissfraktur an den Malleolen oder dem Caput fibulae.
Beim muskelgeführten Gelenk kann es z. B. durch Insuffizienz der
haltgebenden Muskeln (auch in Verbindung mit einer Unterentwicklung des
Labrum glenoidale beim Schultergelenk) zu einer habituellen Luxation
kommen. Dagegen haben auf Gelenken mit Bänderführung
einwirkende Luxationen meist Kapsel- und Bänderrisse zur Folge.
[zurück
zum Inhaltsverzeichnis]
©
Urheber- und Autorenrechte national und international für Texte
und Abbildungen by
Friedrich Ch. Horn, D-87672
Roßhaupten